COMPOSE 3: Langetermijnveiligheid en -werkzaamheid van naldemedine bij chronische niet-kankergerelateerde pijn en OIC
Opioïd-geïnduceerde obstipatie (OIC) is een veelvoorkomende en belastende bijwerking waar veel patiënten die langdurig opioïden gebruiken mee te maken krijgen.1 Naldemedine is goedgekeurd voor de behandeling van OIC bij volwassenen die eerder zijn behandeld met een laxeermiddel.2 De COMPOSE-3-studie werd opgezet om de veiligheid en werkzaamheid van naldemedine gedurende een periode van 52 weken te beoordelen bij patienten met chronische niet-kankergerelateerde pijn en OIC.3
Ten grondslag aan OIC ligt de binding van opioïden aan perifere μ-opioïde receptoren in het maagdarmkanaal, wat leidt tot verminderde motiliteit, verminderde vloeistofafscheiding en verhoogde vochtopname.4Naldemedine is een perifeer werkende μ-opioïde receptorantagonist (PAMORA). PAMORA’s zijn, anders dan laxantia, specifiek gericht op het mechanisme dat OIC veroorzaakt zonder de pijnstillende effecten van opioïden te beinvloeden.5De COMPOSE-3-studie was de eerste gerandomiseerde, placebo-gecontroleerde, dubbelblinde fase III-studie waarin de inzet van een PAMORA op de lange termijn werd onderzocht.
Studieopzet
COMPOSE-3 is een gerandomiseerde, dubbelblinde, fase III-studie met parallelle groepen en is uitgevoerd op 195 locaties wereldwijd gedurende 52 weken. Geïncludeerde patienten hadden een leeftijd van 18 tot 80 jaar, gebruikten wegens chronische niet-kankergerelateerde pijn minstens een maand lang een stabiele dosering opioïden, en hadden last van OIC. De volledige in- en exclusiecriteria zijn samengevat in Figuur 1. De deelnemers werden na een screeningperiode van 14-28 dagen gerandomiseerd (1:1) tussen een eenmaaldaagse orale toediening van naldemedine (0,2 mg) of placebo. De studieopzet is weergegeven in Figuur 2.
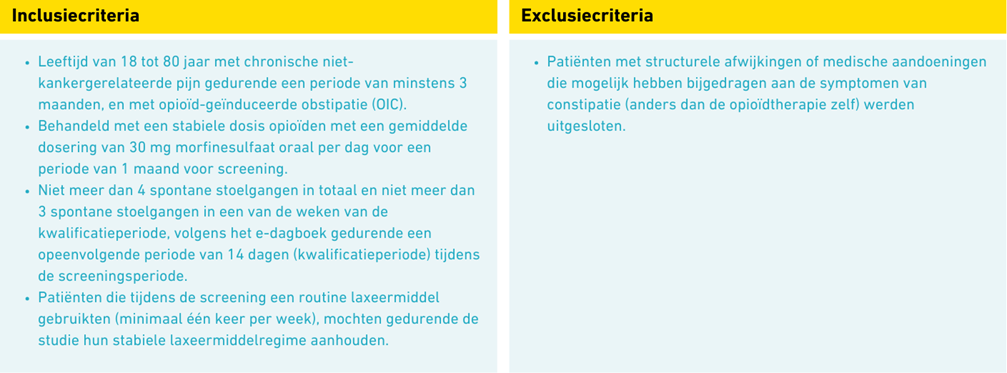
Figuur 1. Belangrijkste in- en exclusiecriteria in de COMPOSE 3-studie.3

Figuur 2. COMPOSE 3 studieopzet3
Uitkomstmaten
De primaire uitkomstmaat was het aantal patienten met bijwerkingen, waaronder ‘treatment-emergent adverse events’ (TRAE’s), ernstige bijwerkingen en bijwerkingen die leidden tot het stopzetten van de behandeling. Belangrijke secundaire uitkomsten waren de mate van opioïd-ontwenningsverschijnselen, de intensiteit van de pijn, de frequentie van de stoelgang, en de kwaliteit van leven van de patient.
Resultaten
Naldemedine wordt goed verdragen
In totaal werden 1.246 deelnemers gerandomiseerd tussen naldemedine (n=623) of placebo (n=623). In de veiligheidsanalyse werden de gegevens van respectievelijk 621 en 619 patiënten meegenomen. Het veiligheidsprofiel van naldemedine was consistent met de resultaten uit eerdere kortdurende studies. Het aantal TRAE’s en bijwerken dat leidde tot het stopzetten van de behandeling was vergelijkbaar tussen de beide groepen.
TRAE’s werden gerapporteerd bij 68,4% van de patienten in de naldemedinegroep versus 72,1% van de placebogroep (verschil [95%-BI]: -3,6% [-8,7-1,5]). Van de patienten in de naldeminegroep moest 6,3% de behandeling staken door bijwerkingen, vergeleken met 5,8% van de placebogroep (verschil [95%-BI]: 0,5% [-2,2-3,1]. Een overzicht van de meest gerapporteerde bijwerkingen is weergegeven in Figuur 3.
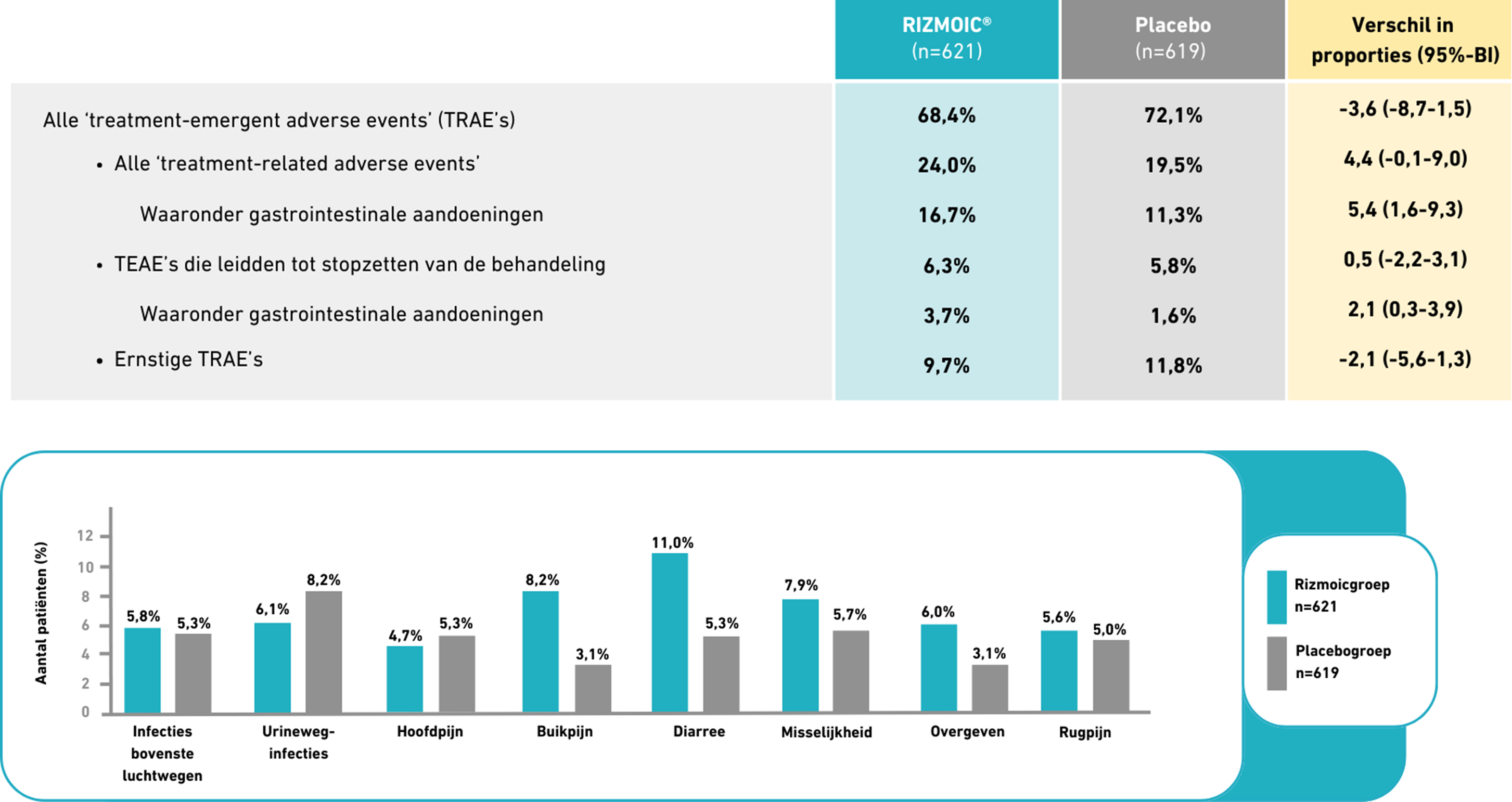
Figuur 3. Overzicht van de belangrijkste bijwerkingen gerapporteerd in de naldemedinegroep en placebogroep3
Aanhoudende effectiviteit
Er waren geen betekenisvolle verschillen tussen groepen in de mate van opioïd-ontwenningsverschijnselen of pijnintensiteit. Behandeling met naldemedine leidde tot aanhoudende significante verbeteringen in de frequentie van de stoelgang, de algehele obstipatiegerelateerde symptomen en kwaliteit van leven ten opzichte van placebo (p=0,0001) op alle tijdstippen.
Conclusie
De resultaten van de COMPOSE-3-studie leveren bewijs ter ondersteuning van het gebruik van naldemedine op de lange termijn voor de behandeling van OIC bij patiënten met chronische niet-kankergerelateerde pijn.
Referenties
- Bell TJ, Panchal SJ, Miaskowski C, Bolge SC, Milanova T, Williamson R. The prevalence, severity, and impact of opioid-induced bowel dysfunction: results of a US and European Patient Survey (PROBE 1). Pain Med. 2009;10(1):35-42.
- Samenvatting van Productkenmerken Rizmoic
- Webster LR, Nalamachu S, Morlion B, Reddy J, Baba Y, Yamada T, Arjona Ferreira JC. Long-term use of naldemedine in the treatment of opioid-induced constipation in patients with chronic noncancer pain: a randomized, double-blind, placebo-controlled phase 3 study. Pain. 2018 May;159(5):987-994.
- Camilleri M, Drossman DA, Becker G, Webster LR, Davies AN, Mawe GM. Emerging treatments in neurogastroenterology: a multidisciplinary working group consensus statement on opioid-induced constipation. Neurogastroenterol Motil. 2014 Oct;26(10):1386-95.
- Weber HC. Opioid-induced constipation in chronic noncancer pain. Curr Opin Endocrinol Diabetes Obes. 2016 Feb;23(1):11-7.
NL-RIZM-2024-00085_NL




